İçerik
- aşamaları
- Yöntem 1 Çözünürlük kurallarını öğrenin
- Yöntem 2 Bir mnemonic kullanın: NAG SAG
- Yöntem 3 Öğrenmenin temelleri
Bir bileşiğin çözünürlüğü, suda çözünme kabiliyetidir. Çözünmeyen bir bileşik, çözeltide bir çökelti oluşturacaktır. Kısmen çözünür bir bileşiğin kimyasal olarak çözünmez olduğu da söylenir. Çözünürlük kurallarını hatırlarsanız, kimyasal denklemlerle çalışmak zorunda olduğunuzda hayatınızı kolaylaştıracaktır. Biraz zaman, iş ve bazı anımsatıcı püf noktaları ile tüm formülleri hatırlayacaksınız.
aşamaları
Yöntem 1 Çözünürlük kurallarını öğrenin
-

Grup 1A tuzları çözünür. Elementlerin periyodik tablosu, sırasıyla "periyot" ve "gruplar" olarak adlandırılan satır ve sütunlarda düzenlenir. Tablonun ilk sütununda 1A grubu elemanları bulunur. Alkali metallerdir. Bunlar Li, Na, K, Cs ve Rb elemanlarını içerir.- Örnek: KCl ve LiOH suda çözünür.
-

Nitratların, kloratların ve asetatların tuzları çözünür. Ne zaman nitrat3), klorat (CIO formülü3) veya lacetate (CH formülü)3COO) tuzları oluşturur, suda çözünürler.- Örnek: KNO3, NaClO3 ve CH3COONaların hepsi çözünür.
-

Tüm amonyum tuzları çözünür. Amonyum aslanı (NH formülü)4su içerisinde tamamen ayrışan tuzları oluşturur. Bu kuralın istisnası yoktur.- Örnek: NH4OH, bir hidroksit iyonu olsa bile çözünür.
-
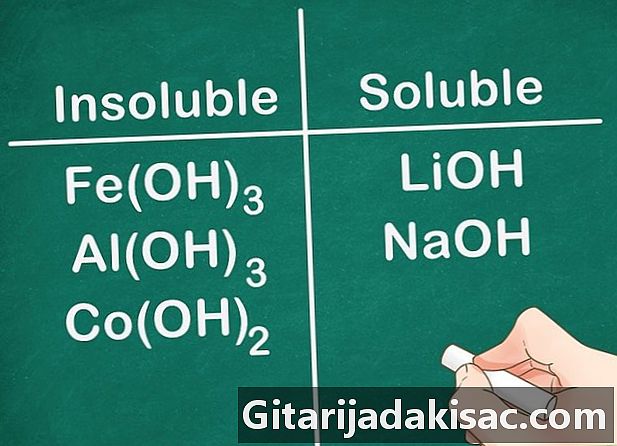
Çoğu hidroksil bileşiği çözünmezdir. Bazı hidroksit tuzları hafif çözünür. Bu, Grup 2 elementleri (Ca, Sr ve Ba) ile oluşturulan hidroksit durumudur. Grup 1 elementleri ile oluşturulan hidroksit tuzları bir istisnadır, çünkü bu elementler hala çözünürdür.- Örnek: Fe (OH)3, Al (OH)3 ve Co (OH)2 çözünmez, ancak LiOH ve NaOH çözünürdür.
-

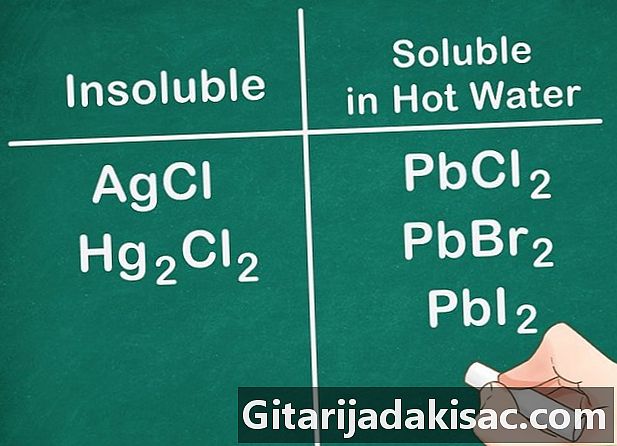
Grup 17 metal olmayan tuzlar genellikle çözülebilir. Grup 17 olmayan metaller arasında klor (Cl), bromid (Br) ve liod (I) bulunur. Para, kurşun ve cıva bu kuralın istisnalarıdır. Bu metal olmayanları ve bu iyonları içeren bileşikler çözünür değildir.- Örnek: AgCl ve Hg2Cı2 ikisi de çözünmez.
- PbCl2, PbBr2 ve PbI2 ÇOK SICAK suda çözünür.
-
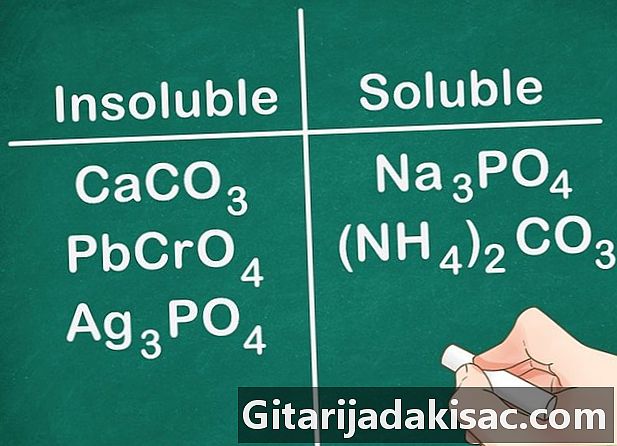
Çoğu karbonat, kromat ve fosfat çözünmez. Bu elementler için kimyasal formüller: CO3 (karbonatlar), CrO4 (kromatlar) ve PO4 (Fosfatlar). Grup 1A metalleri ve NH bileşikleri4 bir istisna ve çözülebilir.- Örnek: CaCO gibi bileşikler3, PbCrO4 ve Ag3PO4 hepsi çözünmez, Na gibi bileşikler ise3PO4 ve (NH4)2CO3 çözünür.
-
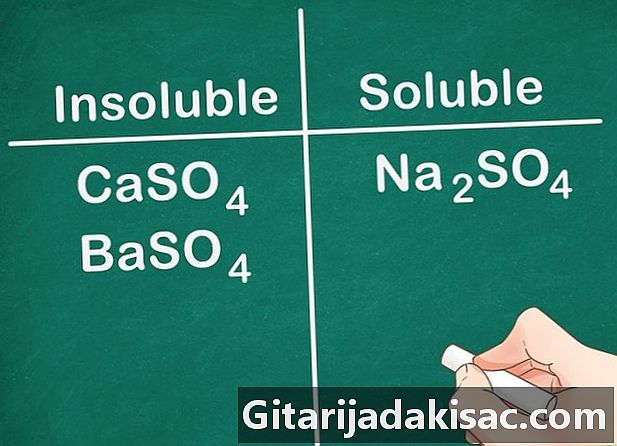
Sülfat tuzlarının çoğu çözünür. SO iyonu içeren çoğu tuz4 Suda çözünür. Ca, Ba, Pb, Ag, Sr ve Hg bu kuralın istisnalarıdır. Bu iyonları içeren sülfat tuzları çözünür değildir.- Örnek: Na2SO4 CaSO iken tamamen çözünür4 ve BaSO4 çözünür değil.
-

Sülfür bileşiklerinin çoğu suda çözünmez. Baryum, kalsiyum, magnezyum, sodyum, potasyum ve amonyum bu kuralın istisnalarıdır. Sadece bu elementlerden ve sülfitten yapılmış bileşikler suda çözünür.- Örnek: CdS, FeS ve ZnS'nin hepsi çözünmez.
- Bununla birlikte, geçiş metali sülfürleri çözünmezdir.
Yöntem 2 Bir mnemonic kullanın: NAG SAG
-

Anımsatıcı NAG SAG anımsatıcısını kullanın. Lacronyme NAG SAG, çözünür bileşikleri ve istisnaları hatırlamak için kolay bir püf noktasıdır. NAG SAG adını yazın ve her harfin anlamını ezberleyin. Bu teknik, tüm çözünürlük kurallarını kapsamaz, ancak bunların iyi bir kısmını kapsar. Tüm harfler çözünür molekülleri temsil eder.- N: Nitratlar (NO3)
- A: Asetatlar (CH3COO)
- G: Grup 1 alkali metaller (Li, Na, vb.)
- S: Sülfatlar (SO4)
- A: Amonyum iyonları (NH4)
- G: Grup 17'nin metal olmayanları (F, Cl, Br, I, vb.)
-

İlk istisna için PMA adını hatırlayın. P, Pb'yi (kurşun) temsil eder. M Merkür'ü temsil eder (Hg2). A, Gümüş'ü (Ag) temsil eder. Bu üç iyon hiçbir zaman sülfat grubu veya grup 17'nin metalitleri ile çözünmez.- Anımsatıcı numarayı not aldığınızda, istisna olduklarını hatırlatmak için PMA kısaltmasının yanına bir yıldız ve SAG'ın S ve G yanlarına benzer bir yıldız çizin.
-

İkinci istisna için "Castro" ve "bar" kelimelerini hatırlayın. Aptalca gelebilir, ancak bu kelimeler kalsiyum iyonlarını hatırlamanıza yardımcı olacaktır (Ca, stronsiyum (Sr) ve baryum (Ba).) Bu üç iyon hiçbir zaman sülfatlarla çözünmez.- Bu kelimelerin yanına bir haç ve SAG'nin S yakınında bir başka hatayı bu iyonların sülfatın çözünürlüğünün istisnaları olduğunu hatırlamak için yapın.
Yöntem 3 Öğrenmenin temelleri
-

Sık sık gözden geçirin. Bilgiyi hatırlamak daima zaman alır ve çalışır. Derslerinizi ne kadar çok okursanız, uzun vadede o kadar çok hatırlarsınız. Kuralları sık sık inceleyin ve konuyla günlük olarak kendinizi test edin.- Öğlen veya akşam yemeğinde arkadaşlarınız veya aileniz hakkında size bu konu hakkında sorular sormalarını isteyin.
- Boş zamanınız olduğunda inceleme için kuralların bir kopyasını elinizde bulundurun.
-

Özet sayfalarını hazırlayın ve kullanın. Kartlar, bir konuyu hızla gözden geçirmek ve ezberlemek için mükemmel bir ortam. Kartlardaki çözünürlük kurallarını bazı örneklerle not edin. Sayfaları, çözünür ve çözünmez bileşiklerin kurallarını ve adlarını öğrenene kadar gözden geçirin.- Kartlarınızı yanınıza alın ve arabada ya da arkadaşlarınızı beklerken incelemeye alın.
- Tüm fırsatlar, girişlerinizi incelemek için iyidir.
-

Anımsatıcı araçları kullanın. Anımsatıcı araçlar, bilgileri hızlı ve kolay bir şekilde ezberlemenize yardımcı olacak ipuçlarıdır. Hatırlatıcı bir terim öğrendiğinizde, hatırlamak için birkaç kez yazmak faydalı olabilir. Anımsatıcı numaralar sadece her harfin ne anlama geldiğini biliyorsanız faydalıdır!- Kısaltmaları ve her harfin ne anlama geldiğini yazma alıştırması yapın.
- İnceleme aşamasındaysanız, ilk önce gelecekteki referansınız için anımsatıcı ipuçlarına dikkat edin.